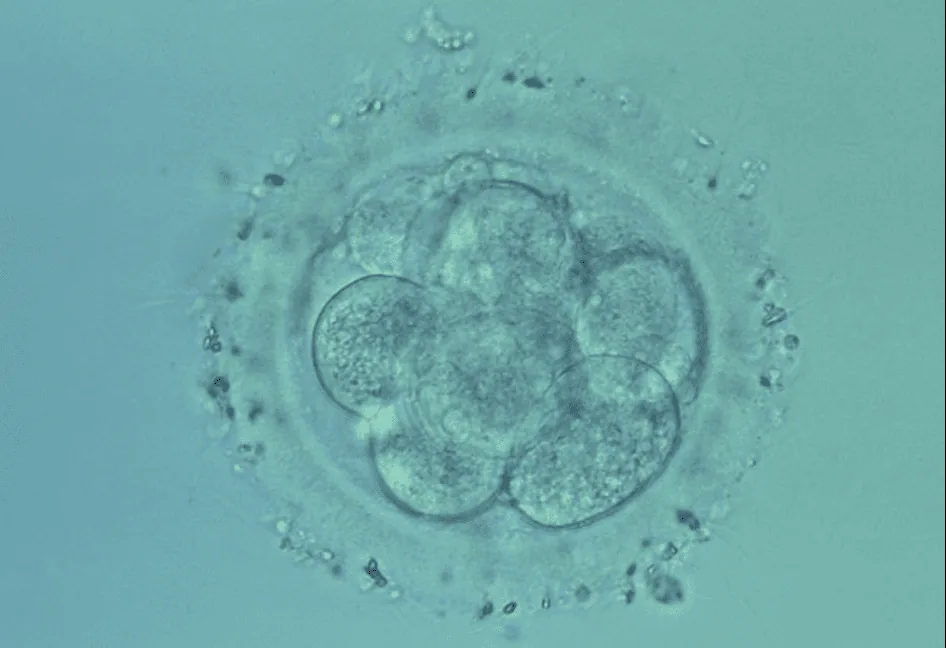
Le DPI-A (Diagnostic PréImplantatoire des Aneuploïdies) est un test génétique réalisé sur l ’embryon obtenu par FIV pour détecter les anomalies du nombre de chromosomes avant le transfert dans l’utérus. Il se distingue du DPI-M (qui recherche une Maladie génétique précise dans une famille à risque). Le DPI-A est interdit en France en 2026, et fait l’objet d’un débat scientifique et éthique relancé par la révision de la Loi de Bioéthique. Cet article décrypte les bénéfices réels, les limites biologiques, le cadre légal, et un angle qui manque dans le débat français : le temps gagné pourrait-il faire la différence sur le nombre d’enfants nés en bout de parcours ?
 Représentation blastocystes en 3 D par le Pr Nathalie Massin
Représentation blastocystes en 3 D par le Pr Nathalie Massin
Dr Nathalie Massin · Gynécologue spécialisée en médecine reproductive · 30 ans d’expérience clinique en consultation hospitalière · Coordinatrice du centre d’AMP de l’Hôpital Américain de Paris · Ex-présidente de la Société de Médecine de la Reproduction · Fondatrice de GynécoLibérée.
Pourquoi cet article maintenant ?
Vous avez peut-être entendu parler des états généraux de la bioéthique 2026, ou lu un article sur le DPI-A dans la presse. Vous vous demandez pourquoi le sujet divise autant, et si c’est vraiment l’examen miracle que certains présentent. Le sujet est complexe parce qu’il mélange trois plans : ce que dit la science, ce qu’autorise la Loi française, et ce que disent les autres pays. Cet article ne tranche pas le débat éthique. Il vous donne les clés pour le lire.
1. Comment fonctionne le test DPI-A lors d’une FIV ?
Aneuploïdie : ce que le dépistage cherche à identifier
Une cellule est dite aneuploïde quand elle présente un nombre anormal de chromosomes (le caryotype normal est de 46 chromosomes, 23 de chaque parent). La trisomie 21 en est l’exemple le plus connu (3 chromosomes 21). Les anomalies chromosomiques affectent le développement et l’implantation d’un embryon, et la majorité des arrêts précoces de grossesse y sont liés. C’est ce que le DPI-A cherche à identifier.
Le protocole technique en 4 étapes
- FIV ou ICSI classique jusqu’au stade blastocyste (cinquième ou sixième jour). À ce stade, deux structures sont distinctes : le bouton embryonnaire (futur fœtus) et le trophectoderme (futur placenta).
- Biopsie du trophectoderme : prélèvement d’environ 10 cellules par le biologiste.
- Vitrification : congélation immédiate de l’embryon (survie supérieure à 95 %).
- Analyse NGS (séquençage de nouvelle génération) des cellules prélevées, puis transfert différé sur le cycle suivant si l’embryon est euploïde.
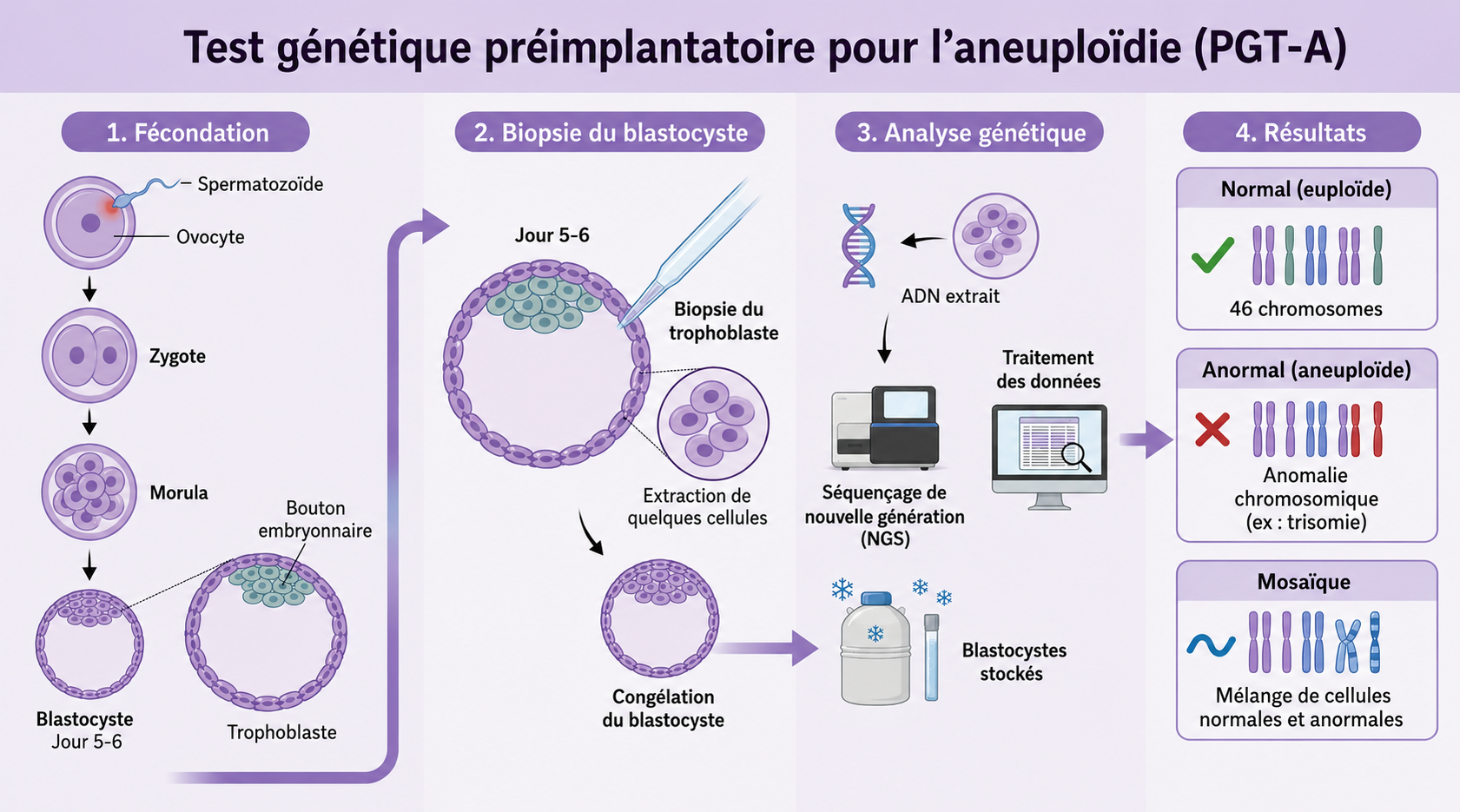 Schéma représentant le processus du DPI-A de la fécondation au résultat génétique sur les cellules du blastocyste par le Pr Nathalie Massin.
Schéma représentant le processus du DPI-A de la fécondation au résultat génétique sur les cellules du blastocyste par le Pr Nathalie Massin.
La différence entre DPI et DPI-A
Le DPI ou DPI-M (sans le A, M pour maladie) est autorisé en France à titre exceptionnel pour les familles à risque élevé de maladie génétique grave (avec un gène malade identifié) ou en cas d’anomalie connue du caryotype : il ne recherche que l’anomalie ciblée. Le DPI-A est un dépistage chromosomique général qui regarde l’ensemble des chromosomes. C’est ce dépistage général qui n’est pas autorisé en France.
2. Bénéfices et limites du DPI-A : ce qu’en disent les études (2024-2026)
C’est ici que beaucoup de femmes en parcours PMA passent à côté de la nuance qui change tout.
Les bénéfices documentés dans les indications ciblées
Pour les patientes ciblées (≥ 35 ans, arrêts de grossesse répétés, échecs d’implantation), les bénéfices sont reconnus par l’ESHRE europénne, la HFEA britannique (2024) et l’ASRM américaine (2024) :
- Moins de grossesses arrêtées : diminution significative du risque de perte de grossesse dans ces populations. Un essai randomisé de référence (Munné, Fertil Steril 2019) a montré chez les femmes de 35 ans et plus un taux de grossesse en cours par transfert significativement augmenté (51 % vs 37 %).
- Moins de transferts inutiles : on évite les essais cliniquement voués à l’échec.
- Réduction du délai de conception : quand un parcours produit plusieurs embryons, le DPI-A permet de transférer en priorité celui qui a le meilleur potentiel chromosomique. Comme le souligne le Dr Thomas Fréour, chef du service AMP au CHU de Nantes : « En sélectionnant celui qui présente le meilleur potentiel, on s’évite des essais infructueux et on raccourcit le délai pour obtenir une grossesse viable. »
Ce qui n’est PAS prouvé : plus de bébés en bout de cycle
C’est le point central, souvent ignoré. Le DPI-A n ’augmente pas le taux de naissance cumulé par cycle commencé. Le grand essai randomisé du NEJM 2021 (Yan et al.) et les analyses en intention de traiter de Munné sont sans appel : quand on compte les naissances par cycle de FIV initié (et non par transfert), le bénéfice disparaît. Pourquoi ? Parce qu’environ 17 % des femmes en protocole DPI-A n’ont finalement aucun embryon transférable, ce qui annule statistiquement le gain par transfert.
3. Le temps gagné, c’est peut-être aussi des enfants gagnés
C’est l’angle qui manque dans le débat français, et qui change la lecture de tout ce qui précède. Mais il demande d’être posé avec rigueur.
Sur un cycle isolé, le DPI-A ne fait pas naître plus d ’enfants.
C’est ce que disent les essais randomisés (Yan, NEJM 2021 ; Munné, Fertil Steril 2019) en intention de traiter, et ce point n’est plus discuté.
Mais un parcours PMA n ’est jamais un cycle isolé. Quand vous avez 38, 40 ou 42 ans, votre fenêtre fertile ne se compte pas en années, elle se compte en cycles. Et chaque cycle qui passe sans donner de naissance, c’est une part de votre stock ovarien qui s’en va. Les données sont sans appel.
À 35 ans, environ 5 à 8 % des femmes en parcours FIV ne produisent aucun embryon euploïde sur un cycle.
C »est un tiers des femmes (33 %) à 42 ans qui repartent sans aucun embryon transférable.
À 44 ans, plus d ’une femme sur deux (53 %), selon une analyse de plus de 15 000 biopsies trophoblastiques (Franasiak, Fertil Steril 2014).
Concrètement, cela veut dire qu’une femme de 40 ans qui économise plusieurs mois sur son parcours grâce à un DPI-A bien indiqué (en évitant un transfert voué à l’échec) peut avoir le temps de tenter un ou deux cycles complémentaires avant que la fenêtre ne se ferme. Et ce sont ces cycles supplémentaires qui, statistiquement, peuvent faire la différence entre rentrer chez soi avec un enfant ou non.
« Le DPI-A ne fait pas naître plus d’enfants par cycle. Mais le temps qu’il fait gagner peut permettre de faire un ou deux cycles supplémentaires. Et c’est peut-être là que se cachent les enfants qui, sans lui, ne seraient jamais nés. »
Existe t-il un bénéfice cumulé sur un parcours complet d’AMP ?
À ce jour, aucun essai randomisé contrôlé n ’a démontré ce bénéfice cumulé sur la durée totale d’un projet bébé. C’est une plausibilité biologique, fondée sur ce que l’on sait du déclin ovocytaire et du déclin de l’euploïdie avec l’âge. Pas un fait scientifique acquis. Cet essai reste à faire.
Cet argument tient sous deux conditions :
- L’âge est avancé (à partir de 38 ans, et surtout 40+)
- L’indication est précise (arrêts de grossesse répétés, échecs d’implantation)
En dessous de 35 ans, sur une première FIV, l’argument ne tient pas. C’est précisément pour ça que les sociétés savantes recommandent le DPI-A dans des indications ciblées et non en routine.
4. Les zones grises : mosaïcisme et biais d’échantillonnage
Le DPI-A donne des résultats qui paraissent binaires (embryon « euploïde » ou « aneuploïde »). En réalité, deux mécanismes biologiques rendent cette dichotomie plus floue qu’elle n’y paraît.
Le mosaïcisme embryonnaire : quand ce n’est ni blanc, ni noir
On parle de mosaïcisme lorsque l’embryon contient au moins deux populations cellulaires de chromosomes différents. Selon la technique de séquençage, entre 3 et 20 % des embryons sont classés mosaïques. Au début, ces embryons étaient systématiquement écartés. Puis des équipes ont tenté leur transfert et des naissances saines ont été obtenues (Greco, NEJM 2015). Le consensus actuel autorise le transfert d’un embryon mosaïque si le mosaïcisme touche moins de 50 % des cellules et un seul chromosome, avec conseil génétique au-delà.
Le biais d’échantillonnage : quand la biopsie ne dit pas tout
C’est l’argument que développe le Pr Stéphane Viville, responsable de l’unité de génétique de l’infertilité à Strasbourg et membre du comité exécutif de l’ESHRE : « Une anomalie constatée dans les cellules trophoblastiques n’entraîne pas automatiquement que le bouton embryonnaire soit affecté. Pourtant, c’est sur cette base que des embryons sont écartés alors qu’ils auraient pu donner des bébés. » Le futur fœtus se développe à partir du bouton embryonnaire, pas du trophectoderme. La biopsie ne le voit jamais directement.
Ces deux mécanismes signifient qu’écarter un embryon sur la base d’un DPI-A comporte une marge d’erreur réelle. Ce n’est pas une science exacte. C’est précisément pour ça que les sociétés savantes recommandent le DPI-A dans des indications précises et non en routine.
5. Pour qui le DPI-A a-t-il un intérêt prouvé aujourd’hui ?
| Indication | Bénéfice attendu | Société savante référente |
|---|---|---|
| Femmes ≥ 35 ans | Diminution du risque de grossesse arrêtée, gain de temps | ASRM 2024, ESHRE, SIFES-MR, HFEA 2024 |
| Arrêts de grossesse répétés | Diminution du risque de récidive | ESHRE, SIFES-MR |
| Échecs d’implantation après plusieurs transferts | Sélection embryonnaire affinée | ESHRE |
| Nombre élevé d’embryons disponibles | Hiérarchisation, raccourcissement du délai | Recommandation pratique |
À l’inverse, les sociétés savantes sont d’accord : le DPI-A ne présente pas d’intérêt en population générale, en première intention, chez les femmes de moins de 35 ans, ni chez les donneuses d’ovocytes. Le faire « par sécurité » dans ces situations peut même réduire les chances de naissance vivante en bout de parcours.
« On parle tout le temps de qualité ovocytaire, de qualité embryonnaire. On parle moins des arrêts de grossesse génétiques liés à une erreur. Et c’est ce que je vis. Trois embryons transférés, deux grossesses arrêtées, et personne ne m’a vraiment expliqué pourquoi. »
Une patiente de 38 ans, en arbitrage France versus Espagne pour un DPI-A.
6. Où faire un DPI-A en Europe ? Espagne, Belgique, Italie
| Pays | Statut du DPI-A | Indications encadrées |
|---|---|---|
| France | Interdit (sauf DPI ciblé : anomalie connue du caryotype ou maladie génétique grave) | Loi de bioéthique 2021, révision prévue en 2027 |
| Espagne | Autorisé | Indications ciblées, accès libéral en pratique |
| Belgique | Autorisé | Encadré par centres agréés |
| Italie | Autorisé | Recommandations SIFES-MR : ≥ 35 ans, arrêts de grossesse répétés |
| Royaume-Uni | Autorisé en complément | HFEA 2024 : technique complémentaire, indications ciblées |
| États-Unis | Autorisé | ASRM 2024 : recommandé dans indications ciblées |
Cette carte explique pourquoi tant de patientes françaises envisagent un parcours PMA à l’étranger quand elles ont une indication potentielle de DPI-A. Sur le décryptage assisté des décisions complexes, voir comment l’IA va changer votre parcours de PMA.
7. Où en est la France en 2026 : Loi de bioéthique 2021
Le cadre légal actuel
La Loi de bioéthique n’autorise l’examen génétique d’un embryon FIV qu’à titre exceptionnel : le DPI ciblé, réservé aux familles à risque élevé de maladie génétique grave avec un gène malade identifié (DPI-M) ou en cas d’anomalie connue du caryotype, dans ce cas seul le chromosome concerné est analysé (pas l’ensemble des chromosomes comme dans le DPI-A).
La loi n’autorise pas à ce jour le DPI-A comme dépistage chromosomique général.
Les états généraux de la bioéthique 2026
Réouverture du débat. Le Pr Samir Hamamah (CHU Montpellier, président de la Fédération française d’étude de la reproduction) plaide pour une autorisation encadrée, réservée à des indications précises. À l’inverse, le Pr Stéphane Viville appelle à maintenir l’interdit, pointant les limites méthodologiques et le manque de preuves robustes en bout de cycle.
En résumé
Le DPI-A n’est ni l’examen miracle ni l’instrument eugéniste que les caricatures décrivent. Il apporte un bénéfice réel mais limité par cycle : moins de grossesses arrêtées, moins de transferts inutiles, dans des indications précises (≥ 35 ans, arrêts de grossesse répétés, échecs d’implantation, embryons nombreux). Pas plus de bébés par cycle initié. Une marge d’erreur biologique réelle. Et un cadre légal français restrictif dont l’évolution se joue maintenant.
L’angle qui manque dans le débat, c’est celui du temps : sur un parcours complet chez les femmes de 38 ans et plus, le temps économisé pourrait permettre un ou deux cycles supplémentaires avant la fermeture de la fenêtre fertile. C’est une plausibilité biologique forte, qui mériterait d’être démontrée par un essai randomisé. Cet essai, en France, attend l’évolution de la Loi pour pouvoir exister.
🕊️ Besoin d’un regard expert sur votre stratégie de fertilité ?
Chaque parcours est unique et le DPI-A n’est qu’une option parmi d’autres. Avant tout, parlez-en avec votre équipe médicale. Et si vous voulez être accompagné·e·s dans votre décision, on regarde votre situation ensemble.
FAQ : questions fréquentes sur le DPI-A
Le DPI-A est-il autorisé en France en 2026 ?
Non. La loi de bioéthique française n’autorise pas le DPI-A en tant que dépistage chromosomique général. Seul le DPI ciblé sur une maladie génétique précise ou une anomalie connue du caryotype est autorisé, dans les familles à risque élevé. Une révision de la loi est en prévue en 2027.
Quels sont les risques d ’un DPI-A pour l’embryon ?
La biopsie au stade blastocyste prélève environ 10 cellules sur le trophectoderme. La vitrification permet une survie embryonnaire supérieure à 95 %. Des effets résiduels sur le développement ne sont pas totalement exclus mais restent à confirmer par d’autres recherches.
Combien d ’embryons faut-il pour faire un DPI-A ?
Il n’y a pas de seuil minimum strict, mais l’intérêt clinique du DPI-A augmente avec le nombre d’embryons disponibles. Avec un seul embryon, le DPI-A apporte peu : si le résultat est anormal, il n’y a plus rien à transférer ; s’il est normal, le transfert aurait eu lieu de toute façon. Une cohorte de plusieurs blastocystes permet une réelle hiérarchisation.
Quelle est la différence entre DPI-M et DPI-A ?
Le DPI recherche une anomalie génétique précise dans une famille à risque connu (mucoviscidose, drépanocytose, anomalie du caryotype parental). Il est autorisé en France à titre exceptionnel. Le DPI-A est un dépistage chromosomique général qui regarde tous les chromosomes. Il n’est pas autorisé en France en 2026.
Le DPI-A fait-il naître plus d ’enfants ?
Sur un cycle de FIV initié, non. Plusieurs essais randomisés (Yan NEJM 2021, Munné Fertil Steril 2019) le montrent. Mais sur la durée totale d’un projet bébé chez une femme de 38 ans et plus, le temps économisé en évitant des transferts voués à l’échec pourrait permettre un ou deux cycles complémentaires avant la fermeture de la fenêtre fertile. Cette hypothèse est biologiquement plausible mais reste à démontrer par un essai randomisé dédié.
Ai-je le droit de demander le transfert de mes embryons mosaïques ?
À l’étranger, oui, dans la plupart des centres. Le consensus international (ESHRE, ASRM) autorise le transfert d’embryons mosaïques si le mosaïcisme touche moins de 50 % des cellules et un seul chromosome. Au-delà, le transfert reste possible avec un conseil génétique préalable. Des naissances saines ont été documentées dès 2015.
Combien coûte un DPI-A à l ’étranger ?
Un package complet (FIV avec biopsie + DPI-A + vitrification + transfert différé) se situe entre 7 000 et 10 000 € en Espagne, un peu plus en Belgique ou au Royaume-Uni. Les coûts d’analyse génétique seuls sont d’environ 2 500 à 4 000 € selon le nombre d’embryons biopsiés.
_Pour comprendre comment cette décision s ’inscrit dans un parcours plus large, voir _ le guide complet du parcours PMA _et l ’article _ comment ne pas opposer fertilité naturelle et AMP.
Dernière mise à jour : mai 2026 · Dr Nathalie Massin · Cet article n ’est pas un avis médical individuel. Les décisions concernant un parcours PMA doivent toujours être prises avec votre équipe médicale.
Sources principales : Yan, NEJM 2021. Munné, Fertil Steril 2019. Greco, NEJM 2015. Franasiak, Fertil Steril 2014 (15 169 biopsies trophectoderme). Recommandations ASRM 2024, ESHRE 2023, HFEA 2024, SIFES-MR 2025. Article La Croix (10/04/2026), Antoine d’Abbundo.
Questions fréquentes sur ce sujet.
Le DPI-A est-il autorisé en France en 2026 ?
Quels sont les risques d ’un DPI-A pour l’embryon ?
Combien d ’embryons faut-il pour faire un DPI-A ?
Quelle est la différence entre DPI-M et DPI-A ?
Le DPI-A fait-il naître plus d ’enfants ?
Ai-je le droit de demander le transfert de mes embryons mosaïques ?
Combien coûte un DPI-A à l ’étranger ?
Vous avez vos bilans en main et vous voulez en parler ?
Découvrir mes offres →